analisisysoluciones2015
martes, 12 de mayo de 2015
diluciones
DILUCIONES
Es una mezcla ya que las cantidades de los componentes no son fijas y también se denomina mezcla por que no hay reacción química en la unión de componentes.
Se denomina Homogénea porque:
Es uniforme ante la observación visual directa o con microscopio, y no apreciamos la existencia de varias partes o fases.
Las partículas de los componentes son de tamaño molecular y están distribuidas sin ningún orden.
Soluto y disolvente:
Es una mezcla ya que las cantidades de los componentes no son fijas y también se denomina mezcla por que no hay reacción química en la unión de componentes.
Se denomina Homogénea porque:
Es uniforme ante la observación visual directa o con microscopio, y no apreciamos la existencia de varias partes o fases.
Las partículas de los componentes son de tamaño molecular y están distribuidas sin ningún orden.
Soluto y disolvente:
La dilución es el procedimiento que se sigue para preparar una disolución menos concentrada a partir de una más concentrada.
Definición general de disolución:Una dilución es una mezcla homogénea, uniforme y estable, formada por dos o más sustancias denominadas componentes. La sustancia presente en mayor cantidad suele recibir el nombre de solvente, y a la de menor cantidad se le llama soluto y es la sustancia disuelta. El soluto puede ser un gas, un líquido o un sólido, y el disolvente puede ser también un gas, un líquido o un sólido.}
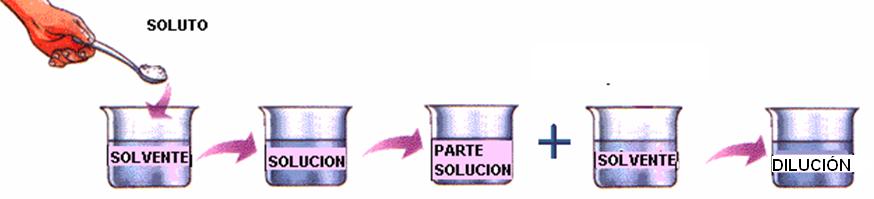
Observadas a través del microscopio, las diluciones aparecen homogéneas y el soluto no puede separarse por filtración.
Se denomina Uniforme puesto que en todas sus partes tiene una misma composición con las mismas propiedades, cojamos la porción de mezcla que cojamos en cada una de ellas siempre encontraremos el mismo contenido en cuanto a sus componentes. Además las partículas se hallan distribuidas de forma ordenada, y no al azar.Se denomina Estable por mantenerse en su composición inicial sin cambiar en cuanto a los componentes químicos que la forman.
Soluto: Es el componente que cambia de fase cuando se produce la disolución; también denominado cuerpo disperso.
Solvente: Es el componente que disuelve, teniendo la propiedad de disolver ciertas sustancias.

domingo, 10 de mayo de 2015
elisa
ELISA
Es el acrónimo en inglés para enzimoinmuno análisis de adsorción y es un examen de laboratorio comúnmente usado para detectar anticuerpos en la sangre.
Forma en que se realiza el examen
La sangre se extrae típicamente de una vena, por lo general de la parte interior del codo o del dorso de la mano. Esto se denomina venopunción.
Preparación para el examen
No se necesita ninguna preparación especial.
Lo que se siente durante el examen
Cuando se inserta la aguja para extraer la sangre, algunas personas sienten un dolor moderado, mientras que otras sólo sienten un pinchazo o sensación de picadura. Posteriormente, puede haber algo de sensación pulsátil.
Razones por las que se realiza el examen
Este examen a menudo se usa para ver si usted ha estado expuesto a virus u otras sustancias que causen infección. Con frecuencia, se emplea para detectar infecciones pasadas o presentes.
Valores normales
Los valores normales dependen del tipo de sustancia que se esté identificando. Los rangos de los valores normales pueden variar ligeramente entre diferentes laboratorios. Hable con el médico acerca del significado de los resultados específicos de su examen.
The examples above show the common measurements for results for these tests. Some laboratories use different measurements or may test different specimens.
Significado de los resultados anormales
Los valores anormales dependen del tipo de sustancia que se esté identificando. En algunas personas, un resultado positivo puede ser normal.
Riesgos
Las venas y las arterias varían en tamaño de un paciente a otro y de un lado del cuerpo a otro; por esta razón, puede ser más difícil obtener una muestra de sangre de algunas personas que de otras.
Otros riesgos asociados con la extracción de sangre son leves, pero pueden ser:
- Sangrado excesivo
- Desmayo o sensación de mareo
- Hematoma (acumulación de sangre debajo de la piel)
- Infección (un riesgo leve cada vez que se presenta ruptura de la piel)
Nombres alternativos
Inmuno análisis ligado a enzimas; Enzimoinmunoanálisis (EIA)
tubidimetria y nefelometria
Turbidimetría y nefelometría
Cuando un rayo de luz golpea una partícula en suspensión, una parte de la luz es reflejada, otra absorbida, otra desviada y el resto es transmitida. La turbidimetría mide la reducción de la intensidad de la luz en su paso a través de una suspensión, a causa de las partículas presentes en esta, y cuantifica la luz residual transmitida. La nefelometría mide la luz desviada en diversos ángulos (entre 15? y 90?) por las partículas presentes en esta suspensión.La sensibilidad de la turbidimetría está limitada, en lo fundamental, por la exactitud y sensibilidad del instrumento utilizado para la medición, y depende de la capacidad del detector para registrar peque?os cambios en la intensidad de la luz. Las lecturas realizadas en longitudes de onda bajas, en un espectrofotómetro de buena calidad, permiten obtener buenos resultados.Para la nefelometría es necesario emplear un equipo con características específicas, que recibe el nombre de nefelómetro. Sus componentes básicos son:- Fuente de luz: los modelos más antiguos empleaban la lámpara de W. En la actualidad se usan lámparas de arco de Hg, diodos emisores o láser de helio-neón, de baja potencia.
- Sistema colimador (innecesario con la lámpara de láser), cuya función es la de concentrar el rayo de luz en haces paralelos.
- Selector de longitud de onda.
- Cubeta de medición.
- Detector (fotomultiplicador).
- Galvanómetro.
Los primeros equipos de este tipo efectuaban la medición de la luz en un ángulo de 90?, pero hoy se prefiere trabajar con la detección en ángulo más peque?o, lo cual confiere una mayor sensibilidad.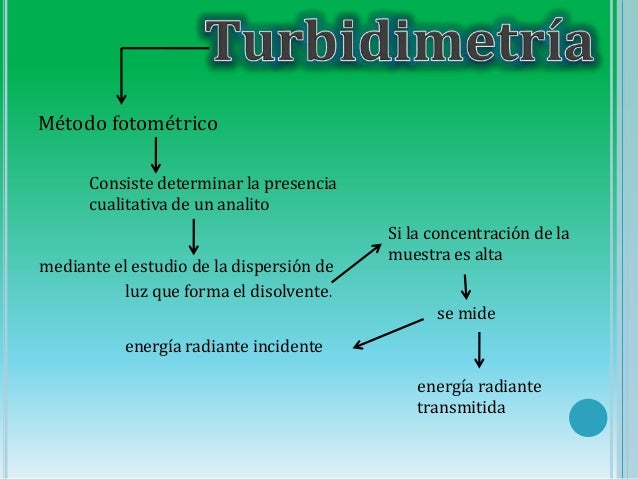
martes, 24 de marzo de 2015
electroforesis
La electroforesis es una técnica para la separación de moléculas según la movilidad de éstas en un campo eléctrico.1 La separación puede realizarse sobre la superficie hidratada de un soporte sólido (p. ej., electroforesis en papel o en acetato de celulosa), a través de una matriz porosa (electroforesis en gel), o bien en disolución (electroforesis libre). Dependiendo de la técnica que se use, la separación obedece en distinta medida a la carga eléctrica de las moléculas y a su masa.
La electroforesis se usa en una gran mayoría en la materia del ADN recombinante ya que nos permite saber la carga que poseen los polipéptidos, y separar los diferentes polipeptidos resultantes de las variaciones del experimento del ADN recombinante. La variante de uso más común para el análisis de mezclas de proteínaso de ácidos nucleicos utiliza como soporte un gel, habitualmente de agarosa o de poliacrilamida. Los ácidos nucleicos ya disponen de una carga eléctrica negativa, que los dirigirá al polo positivo, mientras que las proteínas se cargan al unirse con sustancias como el SDS (detergente) que incorpora cargas negativas de una manera dependiente de la masa molecular de la proteína. Al poner la mezcla de moléculas y aplicar un campo eléctrico, éstas se moverán y deberán ir pasando por la malla del gel (una red tridimensional de fibras cruzadas), por lo que las pequeñas se moverán mejor, más rápidamente. Así, las más pequeñas avanzarán más y las más grandes quedarán cerca del lugar de partida.

Suscribirse a:
Comentarios (Atom)


